A kémia világában a vegyületek rendszerezése elengedhetetlen a megértésükhöz és a velük való munkához. Az egyik alapvető csoportosítási elv a homológ sorok fogalma, amely hasonló szerkezeti felépítésű és kémiai tulajdonságú vegyületek sorozatát jelenti. A telített alkoholok homológ sora kiemelkedő jelentőséggel bír mind az elméleti, mind a gyakorlati kémia szempontjából. Ebben a cikkben részletesen vizsgáljuk meg ezen vegyületek szerkezetét, fizikai és kémiai tulajdonságait, valamint széleskörű felhasználási területeit.
Mi az a homológ sor?
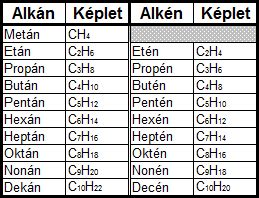
A kémiában az olyan, hasonló szerkezeti képletű vegyületek sorozatát nevezzük homológ sornak, melyek - ugyanazon funkciós csoport jelenléte következtében - hasonló kémiai tulajdonságokkal rendelkeznek, s melyek fizikai tulajdonságait a fokozatos változás jellemzi a molekula méretének és tömegének függvényében. Például az etán forráspontja magasabb, mint a metáné, mivel erősebb Van der Waals- (intermolekuláris) erők jellemzik. Ennek oka a molekulát felépítő atomok számának növekedése. Ilyen, egymástól 14 tömegegységgel különböző homológ sort alkotnak például a telített, nyílt láncú szénhidrogének (alkánok vagy paraffinok), az alkének (olefinek), az éterek és az alkinek (acetilének). A telített, nyílt láncú szénhidrogének, az alkánok homológ sora így kezdődik: metán (CH4), etán (C2H6), propán (C3H8), bután (C4H10) és pentán (C5H12). Hasonlóan épül fel az alkoholok homogén sora. Az egy homológ sorba tartozó vegyületek közös jellemzője, hogy ugyanazt az atomcsoportot, úgynevezett funkciós csoportot tartalmazzák.
Az alkoholok definíciója és szerkezete
Definíció szerint az alkoholok olyan hidroxivegyületek, melyek molekuláiban nyílt láncú vagy gyűrűs, telített vagy telítetlen szénhidrogéncsoporthoz egy vagy több hidroxilcsoport (-OH) kapcsolódik. A hidroxilcsoport a funkciós csoport, amely meghatározza az alkoholok jellegzetes kémiai tulajdonságait.
A fenolok, bár szintén tartalmaznak hidroxilcsoportot, megkülönböztetendők az alkoholoktól. A fenolok esetében a hidroxilcsoport(ok) közvetlenül aromás gyűrűhöz kapcsolódik(nak), míg az alkoholoknál ez a kapcsolódás telített vagy telítetlen szénhidrogéncsoporthoz történik.
Alkoholok csoportosítása
Az alkoholok többféle szempont szerint csoportosíthatók:
- Értékűség szerint:
- Egyértékű alkoholok: Molekulájukban egy hidroxilcsoport található. Például az etil-alkohol (etanol, CH3CH2OH).
- Kétértékű alkoholok (glikolok): Molekulájukban két hidroxilcsoport található. Például a glikol (etán-1,2-diol, H2C(OH)CH2(OH)).
- Hármas- vagy többértékű alkoholok: Molekulájukban három vagy több hidroxilcsoport található. Például a glicerin (propán-1,2,3-triol, H2C(OH)CH(OH)CH2(OH)).

Szénlánc felépítése szerint:
- Telített alkoholok (alkanollok): Szénláncuk csak egyszeres kötéssel kapcsolódó szénatomokból áll.
- Telítetlen alkoholok: Szénláncukban kettős vagy hármas kötés is található.
- Nyílt láncú alkoholok: Szénláncuk lineáris vagy elágazó, de nem zárt gyűrűs.
- Gyűrűs alkoholok (cikloalkoholok): Szénláncuk gyűrűs szerkezetű.
Hidroxilcsoport helyzete szerinti rendűség:
- 1. rendű (primer) alkoholok: A hidroxilcsoportot tartalmazó szénatomhoz csak egy másik szénatom kapcsolódik. Például a bután-1-ol (CH3CH2CH2CH2OH).
- 2. rendű (szekunder) alkoholok: A hidroxilcsoportot tartalmazó szénatomhoz két másik szénatom kapcsolódik. Például az izopropil-alkohol (propan-2-ol, CH3CH(OH)CH3).
- 3. rendű (tercier) alkoholok: A hidroxilcsoportot tartalmazó szénatomhoz három másik szénatom kapcsolódik. Például a tercier izobutil-alkohol (2-metilpropan-2-ol, (CH3)3COH).

Az alkoholok elnevezése általában az alkán neve után az "-ol" végződés hozzáfűzésével történik. A hidroxilcsoport helyzetét számmal jelölik, amennyiben az nem azonosítható egyértelműen az elnevezésből.
Az alkoholok fizikai tulajdonságai
Az alkoholok fizikai tulajdonságait jelentősen befolyásolja a szénlánc hossza és a hidroxilcsoport jelenléte.
Oldhatóság
A kis szénatomszámú alkoholok (metanoltól a butanolig) jól oldódnak vízben. Ennek oka, hogy a hidroxilcsoport képes hidrogénkötést kialakítani a vízmolekulákkal. Az alkoholmolekula apoláris része (a szénhidrogénlánc) és a poláros hidroxilcsoport együttesen határozza meg az oldhatóságot. Ahogy a szénlánc hosszabbodik, az apoláris rész dominánsabbá válik, ami csökkenti az alkohol vízben való oldhatóságát. Ilyenkor az alkohol inkább az apoláris oldószerekben oldódik jobban.
Forráspont és olvadáspont
Az alkoholok forráspontja és olvadáspontja lényegesen magasabb, mint az azonos szénatomszámú alkánoké. Ez a hidrogénkötések kialakulásának köszönhető. Az alkoholmolekulák között kialakuló hidrogénkötések erősebb intermolekuláris erőket jelentenek, mint a csak Van der Waals-erők, amelyek az alkánok között hatnak. Így több energia szükséges a molekulák elválasztásához, ami magasabb forráspontban nyilvánul meg.
A hidrogénkötések kialakulásának képessége az alkoholok forráspontjának növekedését is eredményezi a homológ sorban felfelé haladva. Azonban, ahogy a szénlánc nő, az apoláris jelleg erősödik, így a hidroxilcsoport hatása csökken, és a forráspontkülönbségek kisebbek lesznek a szomszédos tagok között.
A többértékű alkoholok, mint a glikol és a glicerin, még több hidrogénkötést képesek kialakítani, ezért forráspontjuk és olvadáspontjuk még magasabb, viszkozitásuk pedig jelentős.

Az alkoholok kémiai tulajdonságai és reakciói
Az alkoholok kémiai viselkedését elsősorban a hidroxilcsoport polaritása és reakcióképessége határozza meg.
Savasság és bázisság
Az alkoholok általában nagyon gyenge savaknak tekinthetők, még a víznél is gyöngébbek. A hidroxilcsoport oxigénatomjának nagy elektronegativitása miatt az O-H kötés poláros, és elméletileg képes proton (H+) leadására. Azonban ez a savasság rendkívül csekély. Erős bázisokkal, mint a nátrium, reakcióba lépnek, hidrogénfejlődés közben nátrium-alkoholátokat képeznek. Ez a reakció azonban nem tekinthető tipikus sav-bázis reakciónak, inkább redoxi-folyamatnak, ahol a nátrium redukálja a protont hidrogénné.
Etanol reakciója nátriummal
Ugyanakkor az alkoholok oxigénatomja rendelkezik nemkötő elektronpárokkal, ami lehetővé teszi, hogy erős savakkal (pl. HCl, H2SO4) szemben bázisként viselkedjenek. Protonálódnak, azaz elvesznek egy protont a savtól. Ebben a protonált állapotban az alkoholok különleges reakciókban vehetnek részt, például alkil-halogenidek képződésében tömény sósavval való reakció során.
Oxidáció
Az alkoholok oxidációja során aldehidek, ketonok vagy karbonsavak keletkezhetnek, attól függően, hogy milyen típusú alkohollal és milyen oxidálószerrel van dolgunk. A primer alkoholok aldehidekké, majd karbonsavakká oxidálódhatnak, míg a szekunder alkoholok ketonokká. A tercier alkoholok általában ellenállnak az oxidációnak, hacsak nem extrém körülmények között történik a reakció.
Éter- és észterképzés
Az alkoholok reakcióba léphetnek más alkoholokkal vagy savakkal, éterek és észterek képzése céljából. Az éterek az alkoholokból származtathatók, ahol az oxigénatom két szénatomhoz kapcsolódik (R-O-R'). Az észterek pedig karbonsavak és alkoholok reakciójából keletkeznek (R-COO-R').
Fontosabb alkoholok és felhasználásuk
Számos alkoholnak van kiemelkedő jelentősége a mindennapi életben és az iparban.
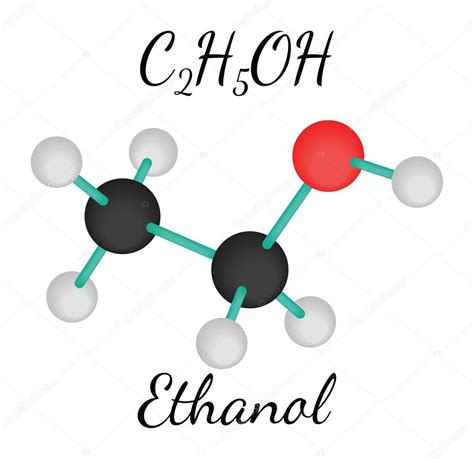
Etanol (etil-alkohol)
Az etanol (CH3CH2OH) az egyik legismertebb alkohol. Víztiszta, kellemes illatú folyadék. Számos iparágban használják:
- Élelmiszeripar és italgyártás: Alkoholos italok alapanyaga.
- Vegyipar: Kiváló oldószer és extrahálószer.
- Üzemanyag: Környezetbarát alternatíva a benzin helyett.
- Fertőtlenítés: Gyakori összetevője a kézfertőtlenítőknek.
Az etanol előállítható fermentációval (szeszes erjedés) cukortartalmú anyagokból, illetve iparilag eténből vagy acetilénből. A denaturálás során emberi fogyasztásra alkalmatlanná teszik, hogy adómentesen lehessen felhasználni ipari célokra.
Metanol (metil-alkohol)
A metanol (CH3OH) az egyszerűbb alkoholok közé tartozik. Kiváló oldószer, energiaforrás és vegyipari alapanyag. Azonban rendkívül mérgező, kis mennyiségben is súlyos látáskárosodást vagy halált okozhat. Korábban főként fa száraz desztillációjából nyerték, ma már főként szintézisgázból állítják elő.
Glikol (etán-1,2-diol)
A glikol (H2C(OH)CH2(OH)) édes ízű, viszkózus folyadék. Jelentős a felhasználása fagyállóként, mivel vizes oldata alacsony hőmérsékleten is folyékony marad. Autók hűtőrendszereiben elterjedten használják.
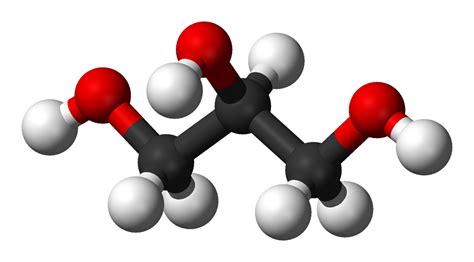
Glicerin (propán-1,2,3-triol)
A glicerin (H2C(OH)CH(OH)CH2(OH)) szintén édes ízű, viszkózus folyadék, amely kiválóan köti meg a nedvességet. Széles körben alkalmazzák a kozmetikai iparban (hidratáló krémek), az élelmiszeriparban, valamint a nitroglicerin előállításában, amely a dinamit egyik fő alkotóeleme.
Fenol (karbolsav)
Bár a fenol nem tekinthető szigorúan alkoholnak (mivel a hidroxilcsoport aromás gyűrűhöz kapcsolódik), fontos megemlíteni kiemelkedő tulajdonságai és felhasználása miatt. A fenol (C6H5OH) színtelen, kristályos anyag, amely mérgező és fertőtlenítő hatású. Vegyipari alapanyagként szolgál gyógyszerek, növényvédő szerek, festékek és műanyagok előállításában.
Összefoglalás
A telített alkoholok homológ sora a kémia egyik alapvető és sokoldalú vegyületcsoportját alkotja. Szerkezetük, fizikai és kémiai tulajdonságaik, valamint széleskörű felhasználási területeik révén nélkülözhetetlenek a modern tudomány és technológia számára. Az alkoholok megértése kulcsfontosságú a szerves kémia és az általunk körülvett világ megismeréséhez.