Az alkoholok a szerves kémia fontos vegyületcsoportját alkotják. Általános jellemzőjük, hogy molekulájukban hidroxilcsoport (-OH) kapcsolódik egy szénhidrogéncsoporthoz. Ezek a vegyületek színtelen, jellegzetes szagú folyadékok vagy szilárd anyagok lehetnek. Az alkoholok semleges kémhatásúak, nem savak és nem bázisok. Molekulaszerkezetük miatt képesek intermolekuláris kölcsönhatásra, különösen hidrogénkötések kialakítására, ami jelentősen befolyásolja fizikai tulajdonságaikat, mint például az oldhatóságot és a forráspontot. Magasabb szénatomszám esetén vízben már nem oldódnak jól, de éterrel, kloroformmal és számos más szerves oldószerrel jól elegyednek.
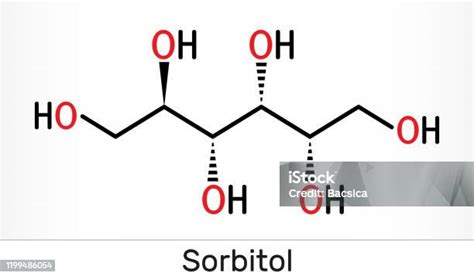
Az etil-alkohol (etanol) a homológ sor második tagja, a metanol után. Ez egy ízletes, könnyen folyó, színtelen folyadék, amelyet széles körben használnak az italok készítésére. Az etanol molekulái képesek másodrendű hidrogénkötések kialakítására, ami magyarázza kiváló oldószer tulajdonságait. Éterrel, kloroformmal, glicerinnel és számos éteres olajjal minden arányban elegyíthető. Gyanták, alkaloidok és számos festék is nagyon jól oldódik benne, bár a ként és a foszfort csak kevéssé oldja. Az etil-alkohol tisztán sosem fordul elő a természetben, mindig híg vizes oldatában található. Előállításának legelterjedtebb módja a cukortartalmú oldatok élesztőkkel való erjesztése.
Az erjesztési folyamat során a keményítőt először alfa-amilázzal kezelik, majd zárt térben felfőzik. A keletkezett cefre kádakba kerül, ahol lehűtik és hozzáadják az amilázt. Az erjedés során keletkező etanolt desztillációval nyerik ki. Az etil-alkohol forráspontja (78 °C) alacsonyabb a víznél (100 °C). Az iparban az etil-alkoholt más vegyületek gyártásához is alapanyagként használják, és üzemanyagként is alkalmazzák, különösen benzinnel keverve. Gyúlékony, de nem anyagkárosító. Azonban a szervezetbe jutva károsítja a májat, a vesét és az idegrendszert, hosszú távon az agysejtek elhalásához és májzsugorodáshoz vezethet.
A metanol, az alkoholok homológ sorának első tagja, a legegyszerűbb telített alkohol. Standard körülmények között kis viszkozitású folyadék, kiváló oldószer. Molekulája viszonylag kicsi. A szervezetben az alkohol dehidrogenáz nevű enzim formaldehiddel alakítja át, ami egy komoly sejtméreg. Ez a formaldehid a metán és más szerves vegyületek oxidációjának köztes terméke, és a szmog egyik összetevője. Szobahőmérsékleten színtelen gáz, vízben jól oldódik. Általában 37%-os vizes oldatban kapható, amely stabilizálóként 10-15% metanolt is tartalmaz. A metanolt belső égésű motorok üzemanyagaként is használják, gyakran benzinnel keverve. Felhasználása más vegyületek szintéziséhez és gyártásához is alapanyagként szolgál. Üzemanyagcellákban történő alkalmazása is várható.
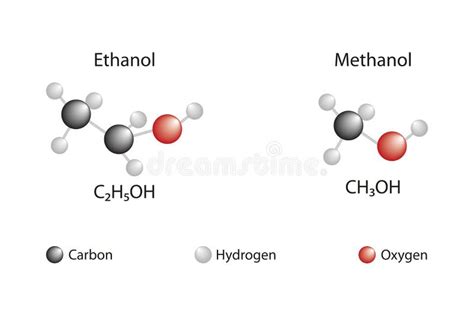
Az oxálsav (sóskasav, etándisav) egy kétbázisú szerves sav, képlete HOOC-COOH. Számos növényben, például sóskában és spenótban megtalálható, valamint az állati szervezetben is előfordul, főleg kalcium-oxalát formájában, ami a vesekövek egyik alkotóeleme. Oxálsav keletkezik sok széntartalmú vegyület, például cukrok oxidációjakor is. Előállítható fűrészporból, kálium- és nátrium-hidroxiddal való hevítéssel, majd kalcium-oxalát képződéssel, amit kénsavval bontanak el. Kisebb mennyiségben glükózból és salétromsavból is előállítható.
Az oxálsav egyhajlású prizmákban kristályosodik, két molekula kristályvizet tartalmazva (H2C2O4·2H2O). Vízben és alkoholban könnyen oldódik, oldata erősen savanyú és savas kémhatású. Oxidáló anyagok, mint a kálium-permanganát, könnyen szén-dioxiddá és vízzé oxidálják, így az oxálsav erős redukálószer. Az iparban karton-, selyem- és gyapotfestészetben, valamint kémiai laboratóriumokban normál oldatok készítésére és oxálsavsók előállítására használják. Nagyobb adagban mérgező a szervezetre. Az oxálsav legegyszerűbben mészvízzel ismerhető fel, amellyel fehér, ecetsavban oldhatatlan csapadékot ad.
Az oxálsav számos sót képez, az úgynevezett oxalátokat. Fontosabbak:
- Kálium-oxalát (K2C2O4·H2O): Vízben könnyen oldódik, barnakő kimutatására és fényképészetben használták. Kálium-hidrogén-oxalát (KHC2O4·H2O) savanyú sója is ismert.
- Kálium-trihidrogén-oxalát (KH3(C2O4)2·2H2O): A sóskasó fő alkotórésze, tinta- és rozsdafoltok eltávolítására használják.
- Kalcium-oxalát (CaC2O4·H2O): Fehér, por alakú csapadék, vízben és ecetsavban oldhatatlan, de sósavban vagy salétromsavban könnyen feloldódik. A növényi és állati szervezetben, valamint vesekövekben is megtalálható.
- Vas(II)-oxalát (FeC2O4·2H2O): Citromsárga csapadék, amelyet vas(II)-szulfát és kálium-oxalát oldatok elegyítésével nyernek. Vas(II)-oxalát és kálium-oxalát kettős sóját "előhívóként" használták a fotográfiában.
- Vas(III)-oxalát (Fe2(C2O4)3): Fény hatására vas(II)-oxaláttá redukálódik, ezért sötétben kell előállítani.
Bár az etil-alkohol és az oxálsav önmagukban is számos felhasználási területtel bírnak, különösen fontosak a vegyiparban, ahol alapanyagként szolgálnak más vegyületek szintéziséhez. Az alkoholok, mint az etanol, kiváló oldószerek, és fontos szerepet játszanak különféle gyanták, festékek és gyógyszerek előállításában. Az oxálsav és sói szintén értékesek festészetben, fényképészetben és analitikai kémiai célokra.
A két vegyület közötti közvetlen reakciók ritkák a hétköznapi felhasználás során, de elméleti síkon megfontolhatóak. Az oxálsav, mint sav, képes reakcióba lépni alkoholokkal, különösen magasabb hőmérsékleten vagy katalizátor jelenlétében, észtereket képezve. Ezek az oxálsav-észterek szintén fontos vegyületek lehetnek, bár kevésbé elterjedtek, mint az alkoholok vagy az oxálsav sói. Azonban az oxálsav erősen savas jellege és oxidáló tulajdonságai miatt óvatosságot igényel az etil-alkohollal való bánásmód során, mivel az alkohol gyúlékony és reakcióképes.
Hogyan készül az etanol
Az alkoholok és szerves savak, mint az oxálsav, szerves kémia alapvető építőkövei. Megértésük kulcsfontosságú a vegyipar, a gyógyszerészet, az élelmiszeripar és számos más területen folyó kutatások és fejlesztések szempontjából. Az etil-alkohol és az oxálsav kölcsönhatásai és felhasználásai jól illusztrálják a szerves kémia sokszínűségét és gyakorlati jelentőségét.
tags: #oxalsav #etil #alkoholban #oldva