Az etanol, vagy közismert nevén etil-alkohol, egy szerves vegyület, amely hidroxilcsoportot (-OH) tartalmaz. Kémiai képlete C₂H₅OH, konstitúciója CH₃-CH₂-OH. A mindennapi életben gyakran csak „alkohol”-ként vagy „szesz”-ként hivatkozunk rá, különösen az alkoholos italok kapcsán. Triviális neve, a borszesz, arra utal, hogy korábban a vegyipar is cukortartalmú anyagok erjesztésével állította elő. Ez a színtelen, jellegzetes illatú és ízű folyadék rendkívül sokoldalú, és számos területen játszik kulcsszerepet, az élelmiszeripartól a gyógyszerészeten át az üzemanyagokig.
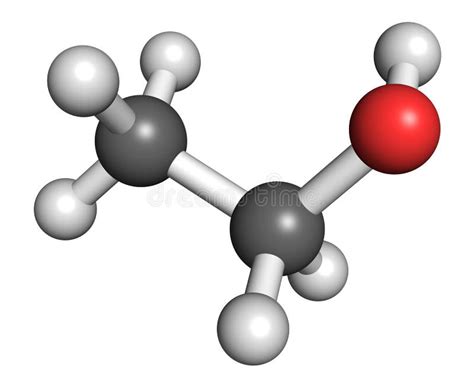
Az etanol molekuláris felépítése és fizikai tulajdonságai
Az etanol molekulája két szénatomot, hat hidrogénatomot és egy oxigénatomot tartalmaz. A szénatomokhoz kapcsolódó hidrogénatomok, illetve a hidroxilcsoport révén az etanol molekulája poláris jelleggel bír. Ez a polaritás, valamint az erős intermolekuláris hidrogénkötések kialakításának képessége határozzák meg fizikai tulajdonságait.
Szobahőmérsékleten és normál légköri nyomáson az etanol színtelen, átlátszó, könnyen folyó folyadék. Jellegzetes, édeskés, de szúrós szagú, tiszta formában pedig csípős ízű. Forráspontja 78,37 °C, ami magasabb, mint sok más szerves oldószeré, de alacsonyabb a víznél. Ez a különbség teszi lehetővé a desztillációval történő elválasztást, ami az alkoholos italok előállításának egyik alapvető lépése. Sűrűsége 20 °C-on 0,789 g/cm³, ami lényegesen kisebb a víznél, ezért az alkoholos italok könnyebbek a víznél.
Az etanol rendkívül jól elegyedik vízzel minden arányban. Ez a kiváló oldhatóság a hidrogénkötések kialakulásának köszönhető, és ez az alapja az alkoholos italok széles skálájának előállításának is. Az etanol a vízzel való elegyítésekor térfogatcsökkenés (kontrakció) figyelhető meg, szintén a hidrogénkötések miatt. Emellett jól elegyedik számos más poláris és apoláris oldószerrel is, például éterrel, kloroformmal, glicerinnel és éteres olajokkal, ami széleskörű oldószerként való felhasználását teszi lehetővé. A molekula egyaránt tartalmaz poláris (hidroxilcsoport) és apoláris (etilcsoport) részeket, ami magyarázza a széleskörű oldóképességét.
Az etanol gyúlékony folyadék, gőzei levegővel robbanásveszélyes elegyet alkothatnak. Lángja kékes és gyakran nehezen látható, ami fokozott óvatosságot igényel a kezelése során.
Az etanol kémiai reakciói és szintézise
Az etanol kémiai tulajdonságai nagymértékben a benne található hidroxilcsoportnak köszönhetők. Számos reakcióban vesz részt, amelyek alapvető fontosságúak ipari előállítása és további vegyületek szintézise szempontjából.
- Égés: Az etanol éghető, és teljes égése során szén-dioxid és víz keletkezik, jelentős energia felszabadulása mellett.
- Oxidáció: Enyhe oxidáció során, például réz-oxid katalizátor jelenlétében, acetaldehiddé (etanol) alakul. Erélyesebb oxidáció hatására ecetsavvá (etánsav) oxidálódik.
- Dehidratáció: Az etanolból vízmolekula eltávolításával (dehidratáció) etén (etilén) keletkezik. Magasabb hőmérsékleten és savas katalizátor jelenlétében két etanolmolekula reagálhat egymással, és dietil-éter (éter) képződik. Ez az éter egy fontos apoláris oldószer, amelyet régebben altatásra is használtak. Az éterek jellemző funkciós csoportja az étercsoport, amely két szénatomot összekötő oxigénatom.
- Észterképzés: Az etanol karbonsavakkal reagálva észtereket képez, például etil-acetátot. Ez a reakció reverzibilis, és savas katalizátor (pl. kénsav) gyorsítja. Az észterek jellemzően kellemes, gyümölcsös illatú vegyületek, amelyeket az élelmiszeriparban, kozmetikában és parfümgyártásban használnak.
- Reakció fémekkel: Gyenge savként viselkedik, és reakcióba léphet aktív fémekkel, például nátriummal, hidrogénfejlődés közben nátrium-etilát (nátrium-etoxid) keletkezik.
Az etanol előállításának két fő módszere van:
- Biológiai fermentáció (erjesztés): Ez a legrégebbi és legelterjedtebb módszer, különösen az alkoholos italok és a bioetanol gyártásában. Cukortartalmú vagy keményítőtartalmú anyagok (pl. szőlő, gyümölcsök, gabonafélék, cukornád, cukorrépa) erjesztésével állítják elő élesztőgombák (pl. Saccharomyces cerevisiae) segítségével. A fermentáció során a szőlőcukor (glükóz, C₆H₁₂O₆) vagy más egyszerű cukrok alakulnak át etanolla és szén-dioxiddá. Keményítőtartalmú alapanyagok esetén először enzimatikusan (pl. alfa-amiláz) alakítják át a keményítőt cukrokká. A fermentációval legfeljebb 15-18% (V/V) etanoltartalmú oldat állítható elő, mivel az élesztőgombák ennél töményebb alkoholban elpusztulnak. Az ennél töményebb alkoholt desztillációval nyerik.
- Ipari szintézis (etilén hidratálása): Nagy tisztaságú, szintetikus etanol előállítására használják. A kőolajpárlatokból származó etilén (etén, C₂H₄) vízzel reagál savas katalizátor (pl. foszforsav, kénsav) jelenlétében, magas hőmérsékleten és nyomáson. Régebben a földgázból előállított acetilénből is előállították.

Az etanol előállítása és tisztítása
A hagyományos fermentációs eljárással előállított „cefre” vagy „sör” az etanol kinyeréséhez és koncentrálásához desztillációt igényel. Mivel az etanol forráspontja (78 °C) alacsonyabb a vízénél (100 °C), a desztilláció során az etanol nagyobb arányban párolog el. Az egyszerű desztillációval előállítható legtöményebb etil-alkoholos oldat „tiszta szesz” (96 V/V%-os), mivel az etanol és a víz azeotrópos elegyet képez, ami együtt forr.
Nagyobb tisztaságú, abszolút (100%-os) etanol előállításához speciális eljárásokra van szükség. Ilyen az azeotrópos desztilláció benzol vagy ciklohexán hozzáadásával, amelyek egy hármas azeotróp elegyet képeznek az alkohollal és vízzel, alacsonyabb forrásponttal. Másik módszer a zeolitok használata, amelyek szelektíven megkötik a vízmolekulákat a nagyobb méretű etanol molekulákból.
Az emberi fogyasztásra szánt alkohol (pl. pálinka) előállítása során a desztilláció mellett további tisztítási lépésekre is szükség van. A réz (vörösréz) tartalmú lepárlókban a kénszármazékok megkötődnek. Fontos lépés az „előpárlat” elkülönítése, amely a fermentáció során keletkező acetaldehid és más, nagyobb szénatomszámú alkoholok (kozmaolajok) nagy részét tartalmazza. Az acetaldehid forráspontja 20 °C, illékonysága nagy, így hamar kiválik az etanolhoz képest. Érdekesség, hogy a metanol, bár forráspontja alacsonyabb (65 °C), elkülönítése az etanoltól kisüsti rendszerű desztillálókkal nehézkes lehet, mert illékonysága megközelítőleg azonos az etanoléval.
Régebben a nem használt, oxidálódott (zöld rézrozsda, grünspan) felületű réz lepárlóknál az alkohol oxidálódott acetaldehiddé, ami az „rézeleje” párlatot adta. Ez a folyamat valójában nem redukció, hanem oxidáció.
A nem emberi fogyasztásra szánt etanolt denaturálószer hozzáadásával teszik fogyasztásra alkalmatlanná, így elkerülhető az alkoholos italokra vonatkozó adófizetés. A denaturálószerek keserűek, kellemetlen szagúak vagy mérgezőek, megakadályozva az emberi fogyasztást.
Az etanol felhasználási területei
Az etanol rendkívül sokoldalú vegyület, és számos iparágban nélkülözhetetlen.
- Italok készítése: Ez az etanol legismertebb és legősibb felhasználási területe. A sör, bor, pálinka, vodka, whisky és számos likőr alapja az etanol. Az erjedési folyamat során keletkező etanol adja az italok bódító hatását, de befolyásolja azok ízvilágát és aromáját is. A 10-12%-nál töményebb alkoholos italokat desztillációval nyerik.
- Üzemanyag: Az etanol egyre nagyobb jelentőséggel bír megújuló üzemanyagként, különösen a bioetanol formájában. Megújuló biomassza forrásokból (kukorica, cukornád, búza, cellulóz) állítják elő fermentációval. Önmagában vagy benzinnel keverve használják gépjárművek hajtására (pl. E10, E85). A bioetanol égése elméletileg szén-dioxid semleges, mivel a növények növekedésük során megkötik a légkörből a CO₂-t. Az E85 oktánszáma magas (104-105), de fűtőértéke alacsonyabb a benzinénél.
- Oldószer: Az etanol kiváló oldószer, amely képes feloldani poláris és apoláris anyagok széles skáláját.
- Gyógyszeripar: Aktív hatóanyagok és segédanyagok oldására használják gyógyszerek, tinktúrák (pl. jód tinktúra) és kivonatok készítése során.
- Kozmetikai ipar: Parfümök, dezodorok, hajlakkok és krémek alapanyagaként funkcionál, illatanyagok és egyéb összetevők hordozójaként.
- Festék- és lakkipar: Oldószerként, hígítóként alkalmazzák.
- Tisztítószerek: Számos tisztítószer összetevője.
- Laboratóriumok: Gyakran használt oldószer, reagens és tisztítószer, kémcsövek és eszközök tisztítására.
- Fertőtlenítőszer: Baktériumölő hatása miatt széles körben használják fertőtlenítésre. Az orvostudományban és a gyógyszeriparban bőrfelületek tisztítására műtétek előtt, injekciók beadása előtt, valamint kéz- és felületfertőtlenítők alapanyagaként. A baktériumok, néhány vírus és gombafajta fehérjéinek denaturálásával fejti ki hatását. A 70%-os etanolos oldat a leghatékonyabb, mivel a víz segíti az alkohol behatolását a sejtfalakba. Azonban az eukarióta parazitákra és baktériumspórákra hatástalan.
- Vegyi alapanyag: Számos más szerves vegyület előállításának kiinduló anyaga, mint például ecetsav, dietil-éter, etil-acetát.
- Élelmiszeripar: Élelmiszer-adalékanyagként használták az élelmiszer-színezékek egyenletes eloszlásának segítésére, valamint élelmiszer-kivonatok ízének növelésére.
Hogyan készül az etanol
Az etanol élettani hatásai és egészségügyi kockázatai
Az etanol, bár széles körben használt és elterjedt vegyület, jelentős élettani hatásokkal rendelkezik az emberi szervezetre, amelyek mind akut, mind krónikus formában megnyilvánulhatnak.
- Felszívódás és hatás: Az etanol a gyomorban és a vékonybélben gyorsan felszívódik a véráramba, és eljut a test minden szövetébe, beleértve az agyat is. Központi idegrendszeri depresszánsként lassítja az agyműködést. Kis mennyiségben eufóriát, gátlások oldódását és relaxációt okozhat, míg nagyobb mennyiségben a koordináció romlását, beszédzavarokat, ítélőképesség csökkenését, memóriazavarokat és álmosságot eredményezhet.
- Alkoholmérgezés: Extrém magas véralkoholszint esetén eszméletvesztés, légzésdepresszió, hányás, hipotermia és akár halál is bekövetkezhet.
- Májkárosodás: Az alkohol lebontása elsősorban a májban történik. A rendszeres alkoholfogyasztás károsítja a májat, ami zsírmájhoz (steatosis hepatis), májgyulladáshoz (hepatitis), és végül májzsugorodáshoz (cirrózis) vezethet.
- Idegrendszeri károsodás: Az alkohol közvetlenül károsítja az agysejteket, ami memóriazavarokhoz, tanulási nehézségekhez és idegrendszeri betegségekhez vezethet.
- Daganatos betegségek: Az alkohol és különösen az acetaldehid (az etanol metabolitja) karcinogén hatású, növelve a szájüregi, garat-, nyelőcső-, máj-, vastagbél- és emlőrák kockázatát.
- Terhesség alatti fogyasztás: Az etanol átjut a placentán és károsítja a fejlődő magzatot, ami magzati alkohol szindrómát (FAS) okozhat, súlyos fizikai és mentális fejlődési rendellenességekkel.
- Alkoholizmus: Az alkoholos italok nagy mennyiségű fogyasztása súlyos mérgező hatással van az emberi szervezetre. Tönkreteszi az idegrendszert, illetve a mérgező anyagok lebontásában fontos májat. Magyarországon jelentős számú idült és enyhébb alkoholista él. Az idült alkoholista olyan mennyiségű alkoholt fogyaszt rendszeresen, amit már elvonási tünetek nélkül képtelen abbahagyni. Az elvonás tünetei lehetnek: vágy, hiányérzet, nyugtalanság, remegés, hideg verejtékezés, szédülés, hallucinációk, görcsök, álmatlanság, idegkimerültség és koncentrációhiány. A leszokást segítő gyógyszerek között néha kemény drogoknak számító nyugtatók is szerepelnek.
A szervezetben az etanol lebontása két fő lépésben történik: először hidrogénelvonással oxidálódik acetaldehiddé, majd további oxidációval ecetsavvá alakul, amelyet a szervezet az anyagcseréje során felhasznál. Rendszeres alkoholfogyasztás esetén először a hasnyálmirigy károsodik, majd a máj is megduzzad. Későbbi stádiumban a máj szövetei elhalnak, helyüket zsírszövet vagy kötőszövet veszi át.
Az alkoholos italok fogyasztása kulturális és társadalmi szokásokkal fonódott össze, azonban fontos tudatosítani a mértéktelen fogyasztás súlyos egészségügyi következményeit.
Környezeti szempontok és a bioetanol
Az etanol, különösen a bioetanol, környezetvédelmi szempontból vegyes megítélésű.
- Szén-dioxid semlegesség: A bioetanol egyik fő vonzereje, hogy szén-dioxid semlegesnek tekinthető. A növények, amelyekből előállítják, növekedésük során megkötik a légkörből a szén-dioxidot a fotoszintézis révén. Amikor a bioetanolt elégetik, ugyanaz a mennyiségű CO₂ kerül vissza a légkörbe, így egy zárt szén-dioxid körforgás jön létre, és elméletileg nem növeli a nettó üvegházhatású gázok kibocsátását.
- Földhasználat és „food vs. fuel” dilemma: Az etanol előállítására szolgáló növények termesztése új területeket igényelhet, ami erdőirtáshoz vagy más természetes élőhelyek pusztulásához vezethet. Amikor élelmiszernövényeket (pl. kukoricát, búzát) használnak üzemanyag előállítására, az felveti az „élelmiszer vs. üzemanyag” dilemmát. Ez a gyakorlat növelheti az élelmiszerárakat, és etikai kérdéseket vet fel a globális élelmiszerbiztonsággal kapcsolatban. A biomassza-alapú bioetanol (pl. cellulózból) előállítása kevésbé terheli az élelmiszer-ellátást.
- Előállítási energiaigény: Bár a bioetanol égése tiszta, az előállítási folyamat (termesztés, betakarítás, szállítás, fermentáció, desztilláció) energiaigényes lehet, és ez befolyásolja a teljes környezeti lábnyomot.
Összességében az etanol egy kettős arcú vegyület: hasznos ipari alapanyag és élvezeti cikk, de felelőtlen fogyasztása súlyos és visszafordíthatatlan egészségügyi károkat okozhat. Környezeti szempontból a bioetanol ígéretes alternatíva lehet a fosszilis üzemanyagokkal szemben, de előállításának módja és a földhasználati kérdések alapos mérlegelést igényelnek.